- +1
哈獸研建立新冠小鼠模型,病毒能同時在上下呼吸道有效復(fù)制
澎湃新聞記者從中國農(nóng)業(yè)科學(xué)院方面獲悉,中國農(nóng)科院哈爾濱獸醫(yī)研究所所長步志高研究員團隊研究建立了能同時在小鼠上呼吸道和下呼吸道穩(wěn)定、有效復(fù)制的新冠病毒SARS-CoV-2感染模型。該研究成果已于8月4日在線發(fā)表在《蛋白質(zhì)與細胞(Protein & Cell)》上,題為“Mouse-adapted SARS-CoV-2 replicates efficiently in the upper and lower respiratory tract of BALB/c and C57BL/6J mice”。

動物感染模型對SARS-CoV-2防治疫苗和藥物研發(fā)及感染與免疫機制研究至關(guān)重要,其中小鼠感染模型具有無可替代的價值。但此前的研究發(fā)現(xiàn),自然情況下,小鼠對SARS-CoV-2不易感,表達SARS-CoV-2入侵細胞受體—人血管緊張素轉(zhuǎn)換酶2(hACE2)轉(zhuǎn)基因小鼠顯著提高了SARS-CoV-2易感性,但也導(dǎo)致包括大腦在內(nèi)的廣泛組織侵噬,作為動物感染模型,與SARS-CoV-2主要感染人類呼吸系統(tǒng)的實際情況存在較大偏離。
因此,研發(fā)出對SARS-CoV-2具有易感性的小鼠感染模型,為深入探索SARS-CoV-2的感染與免疫機制提供了重要手段。
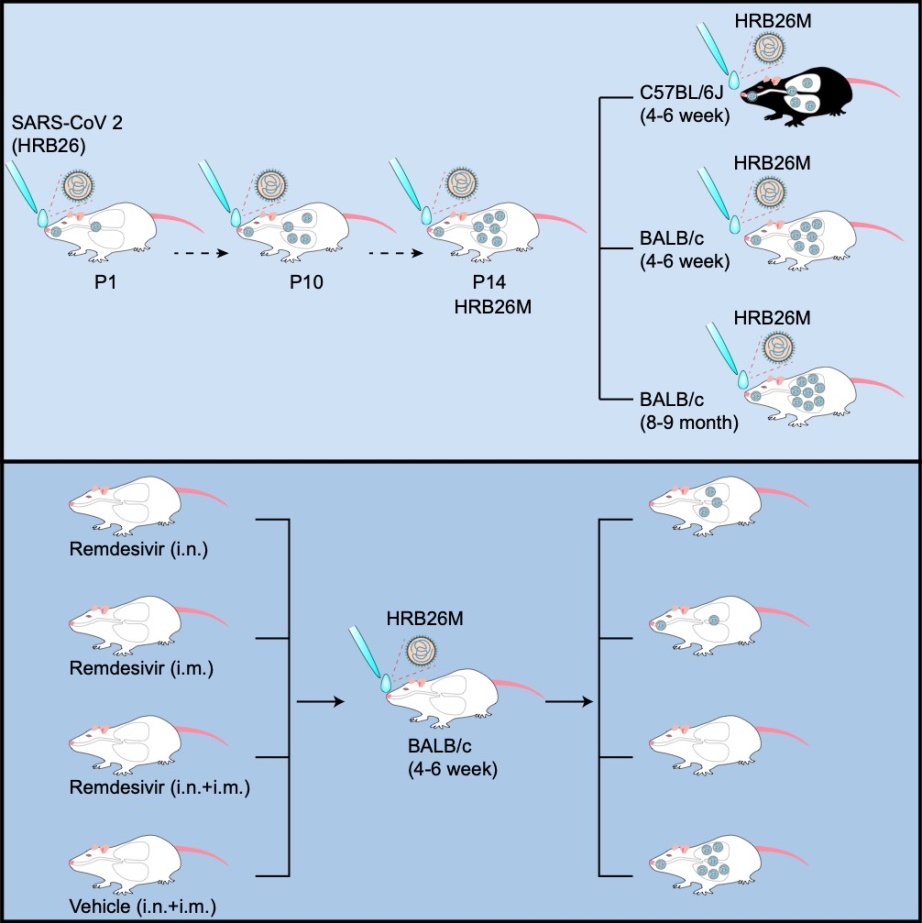
研究團隊此次利用臨床樣品中分離的SARS-CoV-2病毒株(SARS-CoV-2/HRB26/human/2020/CHN (HRB26)),通過鼻腔途徑感染4-6周齡BALB/c小鼠,快速傳代14代,獲得一株小鼠適應(yīng)的SARS-CoV-2(HRB26M),感染后第3天和5天鼻甲和肺臟均檢測到高水平的病毒復(fù)制,并且在8-9月老齡BALB/c小鼠引起典型的肺炎病變。
比較HRB26和HRB26M基因組,研究團隊發(fā)現(xiàn)小鼠適應(yīng)導(dǎo)致3處氨基酸位點突變和一處缺失,分別為nsp8蛋白A81T,S蛋白Q498H和N969S,以及S蛋白中臨近裂解位點的675-679位(QTQTN)缺失。
同時,研究團隊通過體外病毒感染細胞抑制試驗證實,小鼠適應(yīng)突變沒有改變病毒對抗病毒藥物瑞德西韋(Remdesivir)的敏感性。
利用適應(yīng)株HRB26M建立的小鼠感染模型,研究團隊評價了瑞德西韋不同給藥途徑抑制SARS-CoV-2的體內(nèi)效應(yīng),證實肌注和滴鼻聯(lián)合給藥可完全阻止病毒在鼻甲和肺臟的復(fù)制。結(jié)果提示,臨床上使用瑞德西韋治療新冠患者時,應(yīng)考慮聯(lián)合使用肌注和滴鼻兩種給藥方式。
步志高介紹,該BALB/c近交系小鼠是背景最為清晰、應(yīng)用最為廣泛、研究最為深入的實驗動物,其感染模型的建立,為新冠肺炎候選疫苗和抗病毒藥物的大規(guī)模遴選與評價開辟了巨大的研究資源。C57BL/6J小鼠是目前最常用的基因敲除背景小鼠品系,其感染模型的建立,為深入探索新冠病毒的感染與免疫機制提供了重要手段。
博士后王金良、帥磊、王翀和劉任強為該論文共同第一作者,除步志高外,溫志遠研究員和鐘功勛研究員為共同通訊作者。
原文鏈接:https://link.springer.com/article/10.1007%2Fs13238-020-00767-x





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯(lián)網(wǎng)新聞信息服務(wù)許可證:31120170006
增值電信業(yè)務(wù)經(jīng)營許可證:滬B2-2017116
? 2014-2025 上海東方報業(yè)有限公司




