- +1
國家級肥胖癥診療指南來了,提醒GLP-1減肥藥反彈風險

繼“體重管理年”實施方案后,減重領域又迎來了一個國家級指南。
10月17日,國家衛健委發布《肥胖癥診療指南(2024年版)》(以下簡稱《指南》),介紹了肥胖的病因、流行病學數據、定義、相關疾病、診療手段等內容。
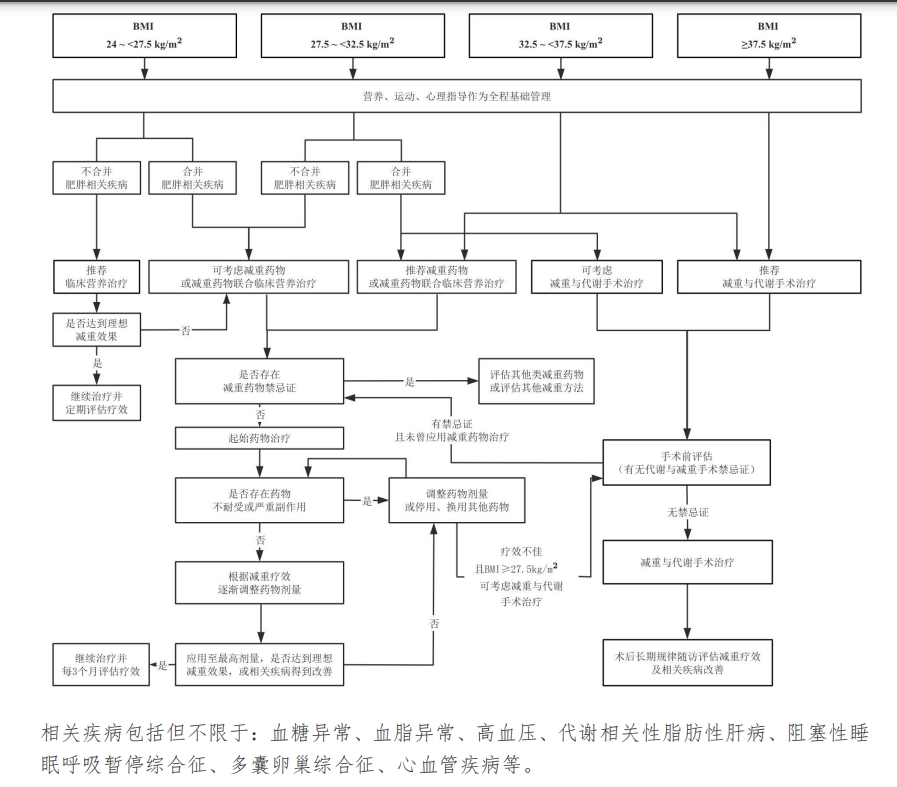
超重和肥胖癥診療路徑 來源:《指南》
根據《中國居民營養與慢性病狀況報告(2020 年)》,按照我國標準,中國成年人(≥18歲)超重率為34.3%,肥胖癥患病率為16.4%,6-17歲青少年兒童超重率和肥胖癥患病率分別為11.1%和 7.9%,6 歲以下兒童的超重率和肥胖癥患病率分別為6.8%和 3.6%。
作為慢性疾病中的獨立病種及多種慢性疾病的重要致病因素,肥胖癥已成為我國重大公共衛生問題,也日益獲得頂層設計的關注。今年6月,國家衛生健康委等16個部門聯合印發《“體重管理年”活動實施方案》,提出自2024年起,力爭通過三年左右時間,實現體重管理支持性環境廣泛建立,全民體重管理意識和技能顯著提升,健康生活方式更加普及,全民參與、人人受益的體重管理良好局面逐漸形成,部分人群體重異常狀況得以改善。
此次發布的《指南》則給出了肥胖癥的權威診療路徑。除了飲食、運動等生活方式干預手段外,藥物和手術是臨床肥胖癥治療的兩大手段。在藥物治療方面,《指南》表示,目前在我國有五種減重藥物獲得國家藥品監督管理局批準用于成年原發性肥胖癥患者減重,包括司美格魯肽、替爾泊肽、利拉魯肽、貝那魯肽、奧利司他,其中前四款均為GLP-1類藥物。

國內已獲批用于治療原發性肥胖癥的藥物比較 來源《指南》
近兩年,GLP-1藥物在全球受到大火,甚至被部分人群奉為“減肥神藥”。《指南》特別提出減肥藥的反彈問題:一項基于美國人群的真實世界數據顯示,在2021年開始使用GLP-1作為減重藥物的患者中,約2/3的患者在1年內因各種原因(包括藥物副作用、經濟負擔、健康保險覆蓋范圍等)停用GLP-1。目前已有部分研究關注了GLP-1停藥后的減重效果,結果均顯示停藥后會出現不同程度的體重反彈,而繼續使用藥物體重可進一步下降。此外,肥胖癥患者對藥物治療的反應存在差異,部分患者通過藥物治療無法達到具有臨床意義的體重減輕(體重降幅至少5%),對于這種情況,建議停止藥物治療。
雖然GLP-1藥物并非萬能“神藥”,但諾和諾德司美格魯肽以及禮來替爾泊肽在商業上的成功,還是讓醫藥行業看到了減肥賽道的巨大商機。今年上半年,諾和諾德司美格魯肽的減重適應證為其全球貢獻了超30億美元的收入。禮來的替爾泊肽減重版上半年全球收入17.61億美元,其中二季度收入12.43億美元。在國內,上述兩款明星減肥產品均已獲批,而不少國內藥企也在推動自家GLP-1藥物在減肥領域的進展。
在仿制藥方面,面臨專利到期的司美格魯肽吸引了多家國內企業跟隨。據insight數據庫顯示,目前,有27家國內企業布局司美格魯肽類似藥/改良型新藥,其中布局肥胖適應證的有13款。
石藥集團(01093.HK)、九源基因等均已申報司美格魯肽生物類似藥的上市,但申報適應證為二型糖尿病,而非減重。翰宇藥業(300199.SZ)則是制劑和原料藥兩條腿走路。9月底,該公司公告稱,收到美國食品藥品監督管理局(FDA)確認,公司司美格魯肽原料藥獲得DMF(Drug Master File)備案號040534。司美格魯肽作為公司國際化布局的GLP-1類的多肽藥物管線產品,本次獲得DMF備案號,提高了公司在國際市場上的競爭力,取得DMF注冊登記號的企業和其產品容易被客戶優先考慮,為公司長期發展帶來積極的影響。
在GLP-1創新藥方面,國內藥企也在奮起直追。10月14日,博瑞醫藥(688166.SH)公告稱,全資子公司博瑞新創自主研發的BGM0504 注射液治療非糖尿病的超重或肥胖的二期臨床試驗達成預期目標。
在15日披露的投資者調研報告中,博瑞醫藥稱,目標劑量給藥第4周時5mg劑量組呈現超過5%的變化,10mg劑量組、15mg劑量組呈現接近10%的變化,起效非常快;目標劑量給藥第24周時5mg劑量組呈現接近11%的降幅,10mg劑量組突破16%的降幅,15mg劑量組呈現接近19%的降幅,而依據文獻數據,司美格魯肽給藥44周及以上降幅水平基本為8.5%-14%,替爾泊肽15mg劑量組海外數據可以超過20%,國內數據高點是15%左右。也就是說,按照博瑞醫藥的說法,從目前的數據來看,其減肥藥的減重效果優于兩大明星品種。
博瑞醫藥還瞄準了減肥藥對血壓的影響這一點。該公司強調,公司結合二期的結果對三期方案做了進一步的優化完善,針對血壓指標公司會在三期臨床進一步考察和評價。海外替爾泊肽、司美格魯肽入組均選擇血壓正常的病人,一般而言肥胖人群中大約有60%會存在高血壓情況,而其入組病人高血壓覆蓋范圍未達到整體肥胖人群的一半,尚未通過完善的臨床試驗來同時解決肥胖和高血壓的問題,這為后來者打開了驗證同時解決肥胖和高血壓臨床需求的空間,產生巨大的差異化市場,這也是一個很值得探索的機會。
信達生物的GLP-1/GCGR雙重激動劑瑪仕度肽也走在國產減肥藥的前列。2024年半年報顯示,瑪仕度肽的兩項NDA已獲NMPA受理,有望很快獲批上市,適應證包括針對肥胖或超重人群的長期體重管理以及治療二型糖尿病。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




