- +14
Nat Commun | 急性應激時如何快速升高血糖?劉際團隊發現HSL軸調節
快速的葡萄糖供應對動物在應激反應中的生存至關重要。下丘腦促腎上腺皮質激素釋放激素(CRH)神經元如何精確控制應激誘導的葡萄糖釋放的時間尺度尚不清楚。
2024年10月5日,中國科學技術大學信息科學與技術學院劉際團隊在Nature Communications 上發表題為《Hypothalamus-sympathetic-liver axis mediates the early phase of stress-induced hyperglycemia in the male mice 》的論文,在該研究中,作者發現應激性高血糖在雄性小鼠中至少可以分為兩個階段:第一個快速階段是由下丘腦(室旁到腹內側下丘腦)-交感神經(白斑中縫核到中外側核)-肝(HSL)軸活動介導的;第二個延遲階段是由腎上腺活動介導的。阻斷HSL軸的活性可削弱捕食誘發的逃跑反應,表明HSL通路的活性是應對應激所必需的。作者進一步揭示了下丘腦CRH信號的胞內級聯,該級聯是由GABAA受體β3亞基在S408/409位點磷酸化介導的,從而阻止GABAA受體膜募集。因此,作者揭示了應激時葡萄糖供應的精確時間尺度,分別由腎上腺非依賴性HSL和腎上腺依賴性途徑介導。

急性應激時,CRH調節快速和延遲的葡萄糖釋放
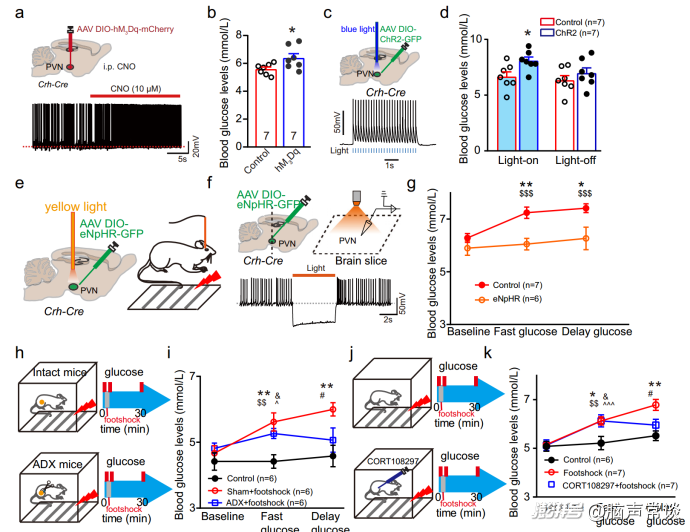
當面對壓力源時,PVN中的CRH神經元被激活,導致腎上腺釋放皮質酮。作者首先詢問PVN中的CRH神經元是否調節葡萄糖水平。為避免攝食引起的血糖變化,實驗前禁食小鼠12小時。通過化學遺傳學方法作者發現,給藥DREADD配體CNO顯著增加CRH神經元的放電率和CRH神經元中c-fos的表達。
與對照組相比,腹腔注射CNO導致實驗組血糖水平升高。為了進一步證實結果,作者采用光遺傳學方法探究PVNCRH神經元的活性。正如預期的那樣,腦切片的體外電生理記錄顯示,當暴露于藍光時,PVNCRH神經元的活性增加。與化學遺傳學數據一致,光刺激CRH神經元導致血糖水平和皮質酮水平顯著升高,這表明PVNCRH神經元的激活確實能夠調節葡萄糖水平。
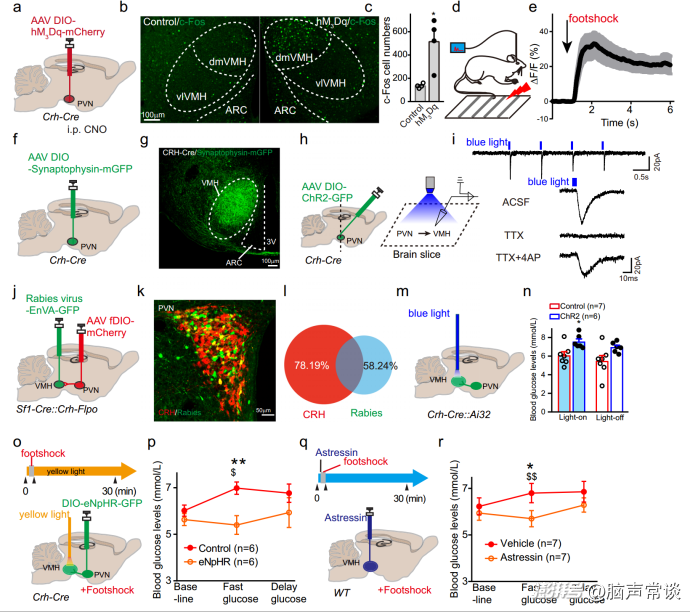
PVNCRH-VMH投射是應激時葡萄糖快速釋放所必需的
為了探索CRH神經元可能的下游靶點,作者化學激活了PVNCRH神經元,并對神經元活性標記物c-Fos進行了免疫染色。刺激PVNCRH神經元顯著增加PVNCRH神經元中c-fos陽性細胞數量。有趣的是,作者還發現VMH中c- fos表達增加。SF-1在VMH中特異性表達。為了進一步測試VMH神經元是否參與應激反應,作者通過光纖記錄鈣信號發現在對急性身體應激(包括足部沖擊、水噴霧和尾夾)的反應中,總體Ca2+信號變化20%(用ΔF/F表示)。這表明VMHSF-1神經元確實參與了應激反應。
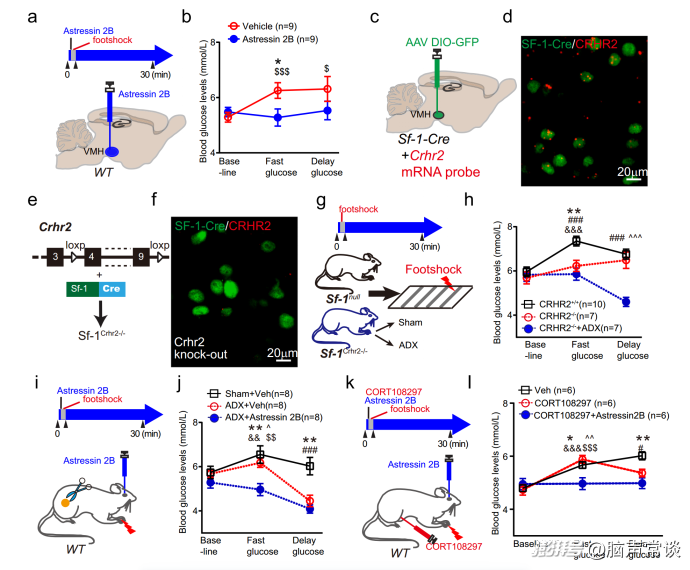
應激時由VMHCRHR2介導CRH啟動的葡萄糖快速釋放
CRHR1和CRHR2均廣泛分布于大腦中,而VMH中CRH受體亞型以CRHR2為主。為了研究CRHR2是否在應激反應中負責葡萄糖調節,作者將不同的CRH受體拮抗劑注入VMH并測量血糖變化。應用CRHR1拮抗劑R121919顯示血糖水平適度變化,而CRHR2拮抗劑Astressin2B與溶劑組相比,在足部休克應激期間阻斷了葡萄糖的快速增加。同樣,Astressin2B在面對水噴、尾夾等其他應激源時,阻斷了葡萄糖的快速升高,但不阻斷延遲期,證實了應激反應中CRH信號介導的高血糖主要是通過VMH中CRHR2的激活介導的。當作者將AAV-DIO-GFP注射到Sf-1-Cre小鼠中標記VMH神經元并使用特異性反義寡核苷酸檢測CRHR2 mRNA時,作者發現大量的CRHR2 mRNA在VMH背內側表達。
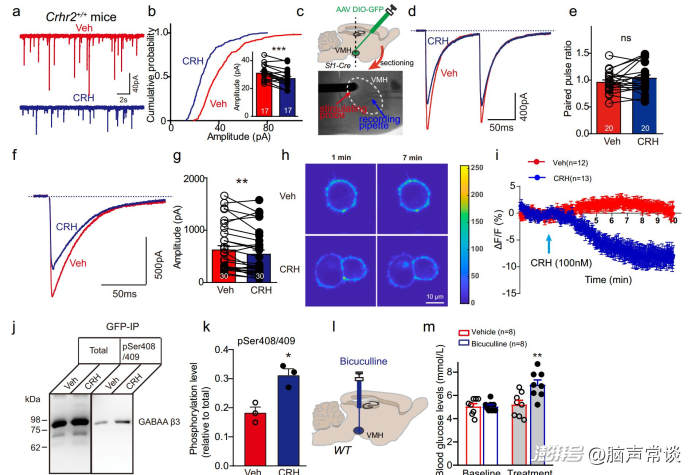
CRH通過VMH中β3 GABAA受體亞基調節抑制性突觸傳遞
作者發現CRH刺激VMH神經元的活動。然而,這種興奮作用是否由突觸傳遞介導尚不清楚。為了回答這個問題,作者采用電壓鉗法記錄VMHSF-1神經元的突觸后電流。CRH的應用不影響自發興奮性突觸后電流(sEPSCs)。而灌注GABAA受體拮抗劑PTX阻斷了CRH對動作電位放電的作用,表明抑制電流可能介導了CRH對VMH神經元活性的影響。事實上,CRH顯著降低了自發抑制性突觸后電流(sIPSCs)的振幅和頻率。同樣,敲除VMHSF-1神經元中CRHr2表達完全降低了CRH誘導的sIPSC幅度和頻率抑制,提示CRHR2激活可抑制SF-1神經元的抑制性張力。

為了可視化GABAARs的細胞表面動力學,作者在N2a細胞系中表達pHluorin(一種ph敏感的GFP變體)標記的GABAAR亞基(β3和γ2)和CRHR2,以實時測量受體的遷移率。作者發現,響應CRH, β3 GABAAR亞基減少,而γ2亞基表達細胞沒有發現顯著變化。這一結果表明,含有β3亞基的GABAAR亞單位是CRH細胞內信號通路的特異性靶點。先前的研究表明,GABAAR亞基的膜轉運很可能通過其胞內域的磷酸化來調節,特別是β3亞基的Ser408/409磷酸化位點。作者發現CRH給藥后,Ser408/409的磷酸化程度顯著增加。這些數據強烈表明,β3 GABAAR亞單位的Ser408/409磷酸化位點是VMH中CRH信號通路的特異性靶點。
下丘腦CRH信號通過HSL軸活性調控葡萄糖的快速釋放
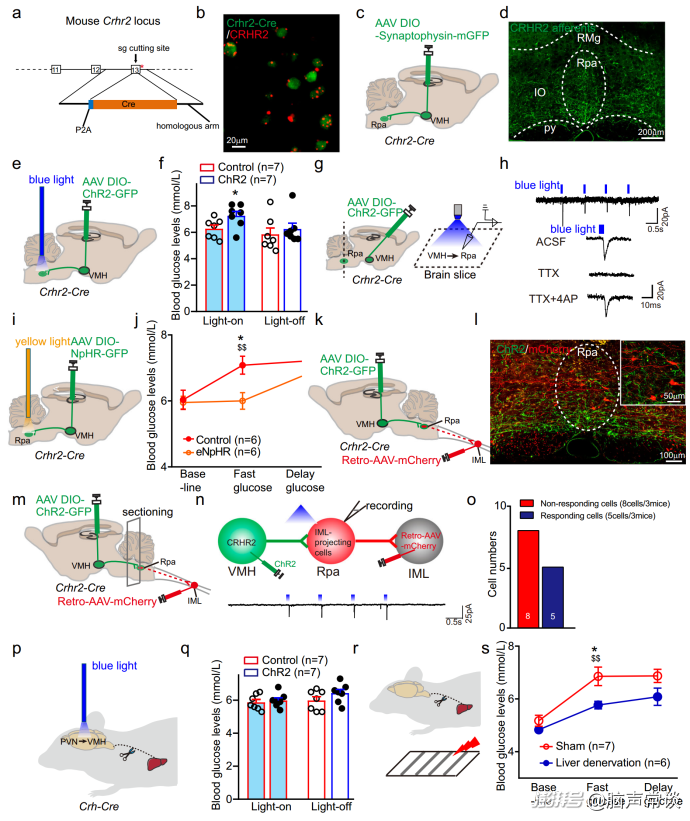
作者之前的研究表明VMH可以通過交感神經通路控制葡萄糖代謝。作者假設VMHCRHR2調節應激誘導的葡萄糖釋放可以通過交感神經傳入肝臟介導。為了驗證這一假設,作者使用CRISPR-Cas9系統構建了CRHr2-Cre小鼠。首先,作者通過在CRHr2-Cre小鼠的VMH中注射順行失蹤病毒發現,在腦干區域,包括迷走神經背運動核(DMV)和蒼白中縫核(Rpa),發現密集的標記終末,在孤束核(NTS)中發現少量纖維。光刺激VMHCRHR2 - Rpa通路可顯著提高血糖。
為了測試VMHCRHR2是否與Rpa神經元形成單突觸連接,作者在CRHR2神經元中表達AAV-DIO-ChR2。在藍光照射下,Rpa神經元中發現了時間鎖定的突觸后興奮電流,該電流可被突觸前阻斷劑TTX阻斷,并被TTX + 4-AP恢復,表明VMHCRHR2與Rpa神經元之間存在單突觸連接。
HSL軸介導的快速葡萄糖釋放對于捕食誘導的飛行反應是必需的
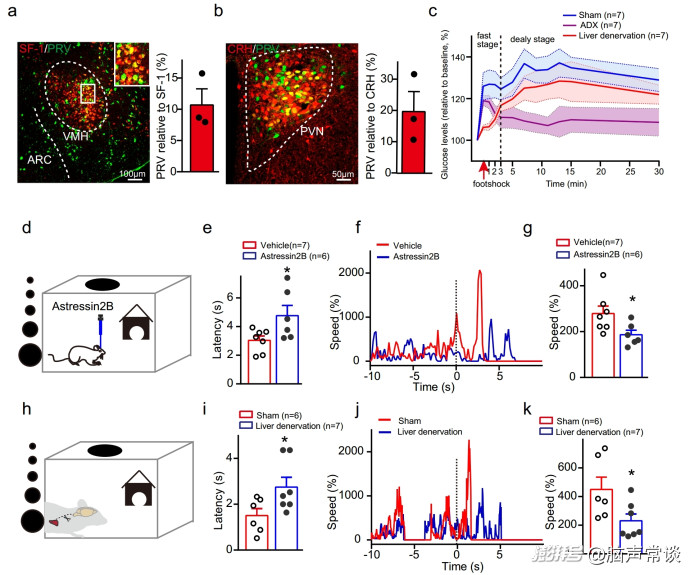
為了進一步證實下丘腦CRH信號與肝臟之間的直接聯系,作者在Sf-1-Cre小鼠的VMH中注射了AAV-DIO-mCherry,并在肝臟中注射了跨突觸逆行示跡劑偽狂犬病毒(PRV)。作者在VMH中發現了大量的GFP+神經元,它們與mCherry標記的SF-1共定位,表明VMH-肝臟存在連接。在PVN中,作者還發現了gfplar標記的肝臟PRV的共定位和CRH的免疫染色,表明PVNCRH -肝臟存在投射。接下來,作者發現HSL軸活性在應激反應的早期(0-3分鐘)是必需的,而腎上腺活性在應激反應的后期(3分鐘)葡萄糖釋放是必需的。
當面臨潛在威脅時,快速能量供應對于動物的生存至關重要。接下來,作者想知道VMH中的CRH信號是否對于捕食性線索誘導的飛行反應是必需的。為了驗證這一假設,作者在VMH中注射了CRHR2拮抗劑Astressin2B。在模擬接近的捕食者時,動物會開始逃逸并躲進巢穴。當通過局部注射Astressin2B阻斷VMH中的CRH信號時,作者發現逃離巢穴的潛伏期延長,飛行速度降低。這表明VMH中的CRHR2對于捕食性線索誘導的飛行反應是必要的。
總結
在本研究中,作者定義了一個下丘腦-交感-肝臟軸,它在應激反應期間獨立于腎上腺活動而介導快速葡萄糖釋放。應激信號通過CRHR2介導的β3 GABAA受體膜招募來調節抑制性張力,從而整合到VMH中,作為血糖水平的中樞控制。
總之,作者發現應激肽CRH啟動了由快速和延遲兩個階段組成的葡萄糖釋放過程,分別由HSL和腎上腺激素調節。早期階段由PVN-VMH-Rpa-交感神經系統介導,在急性應激期間維持快速的葡萄糖供應,這對動物在面對應激源時的生存至關重要。
找實驗方法,上腦聲常談。
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司